血管外傷による急性動脈閉塞は、急性動脈閉塞症の中でも最も重篤な病態です。
四肢、とくに下肢では、受傷後6時間以内に血行再建を行わなければ救肢は不能となり、切断に至ります。
主な原因は交通事故などの外傷であり、救肢には迅速な診断と緊急血行再建が不可欠です。
四肢の血管外傷では、動脈および静脈の損傷に加え、伴走する神経損傷や骨折を合併することが少なくありません。
受傷原因としては、刃物による刺創・切創(図1,2)、鈍器や重量物による挫傷・挫滅〈図3,4〉(作業事故、交通事故)、日本では稀ですが銃創などがあります。最も頻度が高いのは交通事故です〈図5〉。
動脈の切創・刺創では大出血を来し、止血後も損傷部位より末梢側に急性動脈閉塞が生じて壊死が進行します。そのため救急搬送後、速やかな血行再建が必要です。受傷後6時間が救肢の限界です。
骨折を伴う場合には、整形外科により骨折整復を行った後に血行再建を施行しますので、時間的余裕はありません。救肢には血行再建手技に関する高度な経験と多彩な技量が求められ、熟練した血管外科医による治療が不可欠です。
神経損傷が切創であれば、損傷部位に応じて神経縫合を行いますが、優先すべきは血行再建です。
静脈損傷は動脈損傷と比較して緊急性は低く、適切な処置により大きな後遺障害を残さないことが多いです。
損傷部位と受傷機転により重症度は異なりますが、中枢側の損傷ほど重症であり、受傷様式では挫傷・挫滅が最も重篤です。
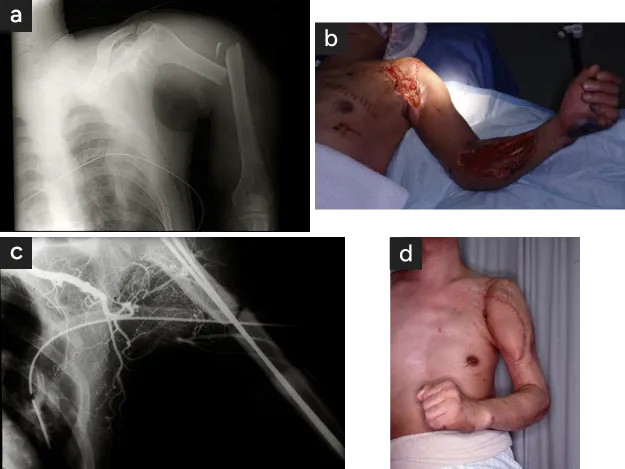
48才/男性
農作業バインダーの刃による刺創、挫創、左腋窩動脈閉塞、上腕骨折、神経挫傷
- 受傷時の骨折所見
- 受傷1週間後の創所見
- 血行再建前動脈造影、腋窩動脈閉塞と修復された上腕骨骨折
- 腋窩動脈再建と遊離筋皮弁移植による救肢1 年後。上肢の運動機能は高度に回復
